|
東京工業大学の本館の前にはウッドデッキがあり、桜が大変綺麗である。学生約1万人が学んでいるが、その内の10%が留学生で、いろいろな言葉が飛び交っている。女子学生は10%と少ないので、増やそうとしているが少しずつしか増えず、男子校の雰囲気が強い。私は35年間つくばの研究所(現、国立研究開発法人
物質・材料研究機構)に勤めたあと、東京工業大学で9年間勤めた。研究室のパンフレットには、許可を得て手塚治虫の火の鳥を載せている。火の鳥はマグマから生まれた命で、私達の研究もセラミックスを高温で焼き命に関わるものである。研究内容は再生医療、ナノメディスン、診断技術。再生医療は細胞や材料を用いて本当の骨に治す医療である。ナノメディスンは副作用を起こさない薬で治療する技術で、ナノテクノロジーとバイオテクノロジーの中間の技術である。診断技術はその場で簡単に安く診断ができる技術開発で、半導体技術を使っている。
本日は骨の再生医療について紹介する。身体の中に入れる人工骨は、医学部だけでも作れないし、工学部だけでも作れないので、医工連携が非常に大事である。患者さんに役立つためには産の支えが必要で、医工産連携が非常に大切であるが、口で言うほど簡単ではなく極めて難しい。そのような話も含めて紹介する。
1.はじめに(骨について)
角砂糖くらいの大きさに切った骨(皮質骨)は、150㎏の相撲取りが乗っても壊れない。多分数人乗っても壊れない。骨は柔軟であるが、非常に強いという不思議な性質を有している。
骨は二つの成分からできている。一つの成分は無機物であり、リン酸カルシウムの一種、水酸アパタイトCa10(PO4)6(OH)2(通常、単にアパタイトという)である。アパタイトは世の中で一番溶け難く、溶解度積は10‐100である。溶け難いということは骨を作り直すのが困難であることになるが、生体は工夫をしている。もう一つの成分は有機物で、たんぱく質の一種であるコラーゲン(棒状分子、アミノ酸)である。人体のたんぱく質の1/3はコラーゲンからできている。アパタイトは大きさ30nmの結晶で圧縮に強く、コラーゲンは長さ300 nmの分子で引っ張りに強い。これらの二つの成分がnmオーダーで綺麗に並んでナノコンポジットを形成するため、骨は押しても引いても強いという特徴を有する。
元気な骨を作るためには、骨の一つの成分となるカルシウムを含むチーズ、ししゃも、えんどう豆などを食べれば良いが、カルシウムが腸から吸収されるのを助けるため、いわし丸干し、しらす干し、さけなどに含まれるビタミンDを摂る必要がある。ビタミンDを摂るだけでは駄目で、太陽に当たることによって皮膚で活性ビタミンDに変化させる必要がある。骨のもう一つの成分であるたんぱく質は豆腐、肉、フカヒレなどを食べると良いが、アミノ酸に分解されて吸収されるので、たんぱく質に変化させるためにはビタミンCを摂る必要がある。
赤ちゃんは生まれたときには頭蓋骨と鎖骨は骨化しているが、その他は軟骨である。脳を守るために頭蓋骨が骨になり、心臓を守るために鎖骨は骨になっていると考えられる。生まれて重力を感じるようになると、軟骨は少しずつ骨に変わっていく。これを内軟骨性骨化という。
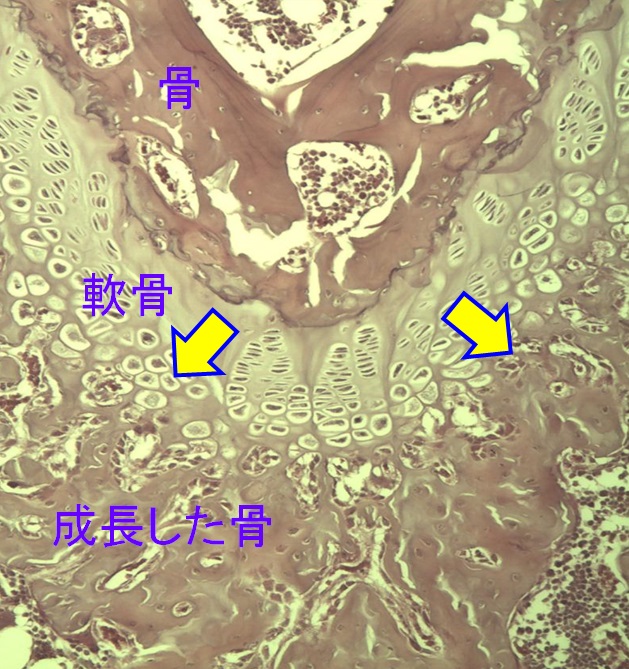 小学生、中学生の骨は骨端線で成長する。子供の骨端線は元気で骨が速く成長する。右図はラットの脛骨の一部を拡大した写真である。「骨」と書いてある部分はV字状の組織であり、それが骨端線である。骨の中にある細胞は、いろいろなものに変わりうる幹細胞で、先ず「軟骨」に変わり、軟骨が「骨」に変わっていく。骨がいきなり成長するのではなく、一度軟骨になってから骨ができる内軟骨性骨化によって成長することが子供達の身体の中で起こっている。高校生になると骨端線が少なく弱くなり、背の伸びるのが止まる。我々のような大人になると骨端線は全くなくなり、骨端線と異なった成長の仕方で骨が作られている。 小学生、中学生の骨は骨端線で成長する。子供の骨端線は元気で骨が速く成長する。右図はラットの脛骨の一部を拡大した写真である。「骨」と書いてある部分はV字状の組織であり、それが骨端線である。骨の中にある細胞は、いろいろなものに変わりうる幹細胞で、先ず「軟骨」に変わり、軟骨が「骨」に変わっていく。骨がいきなり成長するのではなく、一度軟骨になってから骨ができる内軟骨性骨化によって成長することが子供達の身体の中で起こっている。高校生になると骨端線が少なく弱くなり、背の伸びるのが止まる。我々のような大人になると骨端線は全くなくなり、骨端線と異なった成長の仕方で骨が作られている。
骨は作られては壊され、毎日0.3~0.5gのカルシウムを摂ると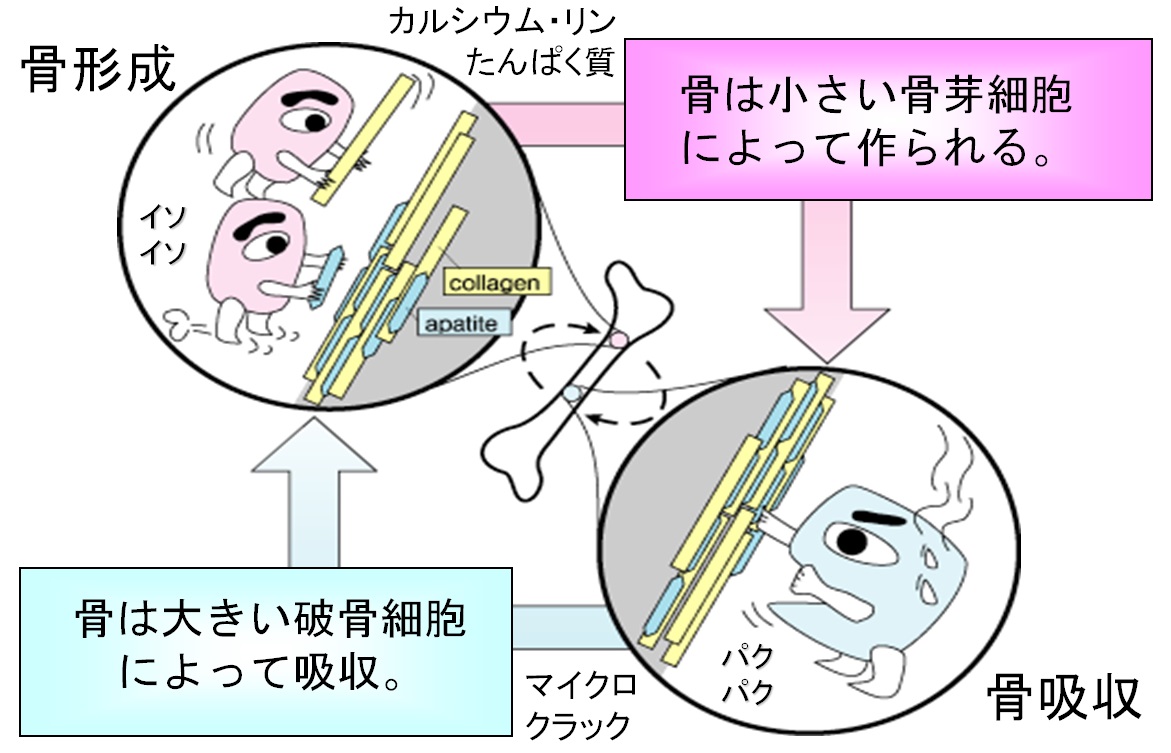 3~5年で全て新しい骨に変わる。骨は小さな骨芽細胞によって作られ、大きな破骨細胞によって吸収される。これを骨のリモデリング(右図)という。若い人は骨を作る骨芽細胞が元気で、骨を壊す破骨細胞も元気であるため、バランスがとれている。しかし年を取ると骨芽細胞は元気でなくなるが、破骨細胞は元気なままであるため、骨量が減り骨は弱くなっていく。骨を作るためには、エストロジェンという女性ホルモンが必要である。女性は閉経後に女性ホルモンが減る。そのために、骨粗鬆症は男性より女性に多い。カルシウムとたんぱく質を摂るのが良く、特に牛乳を飲んで太陽に当たるのが良い。 3~5年で全て新しい骨に変わる。骨は小さな骨芽細胞によって作られ、大きな破骨細胞によって吸収される。これを骨のリモデリング(右図)という。若い人は骨を作る骨芽細胞が元気で、骨を壊す破骨細胞も元気であるため、バランスがとれている。しかし年を取ると骨芽細胞は元気でなくなるが、破骨細胞は元気なままであるため、骨量が減り骨は弱くなっていく。骨を作るためには、エストロジェンという女性ホルモンが必要である。女性は閉経後に女性ホルモンが減る。そのために、骨粗鬆症は男性より女性に多い。カルシウムとたんぱく質を摂るのが良く、特に牛乳を飲んで太陽に当たるのが良い。
2.人工骨のいま!(骨補填材料の現状)
癌などの病気や怪我で骨に欠陥ができると、欠損部に骨補填材を入れる。この材料が骨に変わったり、材料と骨の複合体になったりする。どういう材料が骨補填材に適しているだろうか。
生物は体内に隙間ができることを嫌い、欠損部を埋めるため筋肉側では繊維芽細胞が活躍し、骨側では骨芽細胞が活躍する。繊維芽細胞は骨芽細胞より圧倒的に元気がよく、普通に放って置くと骨は少ししかできず筋肉が欠損部を埋めることになり、骨が弱くなってしまう。そこで、欠損部に骨が再生する環境を作るため骨補填材料を入れる。
骨を再生するためには、①細胞(骨髄の中の間葉系幹細胞やiPS細胞)、②成長因子・サイトカイン(骨を作る細胞に変える薬のようなもの)、③生体材料(細胞外基質である骨に変わるもの)が必要である。骨補填材は30年くらい前から使われ、それが第一世代である。2000年頃から第二世代が出始め、骨再生の補助する材料(高強度多孔体「ネオボーン」、血管侵入性の高い人工骨「リジェノス」)から生体内で本当の骨に変わる再生を促進する材料「リフィット」へと進展してきた。
私達はこれら三つの人工骨の開発に関与してきたが、「リフィット」は基礎研究から実用化までに30年近く掛かり、特に思い入れのある材料である。以下に第二世代の三つの人工骨を紹介する。
(1)高強度多孔体・人工骨「ネオボーン」
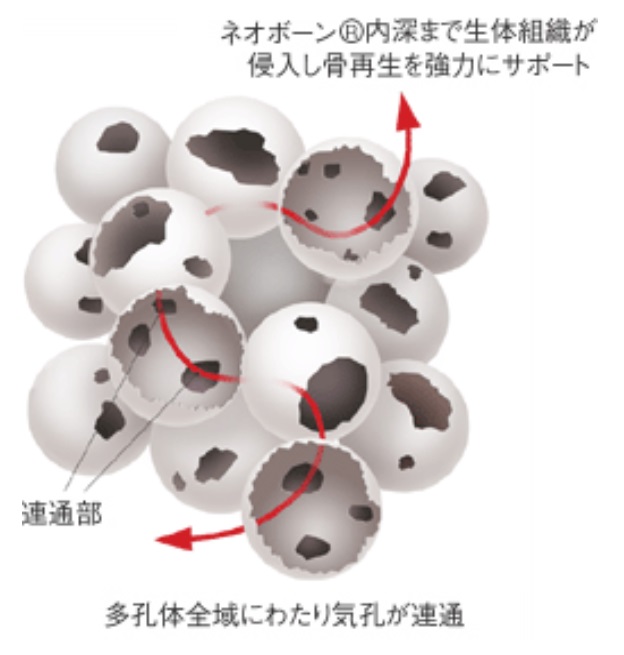
「ネオボーン」という商品名で2003年に東芝電興(現、コパレントマテリアル)から製造・販売された。いろいろな形状のものが出ている。第二世代のものは気孔率が72~78%と高いにも拘らず圧縮強度が12MPaと高い。右図に示すように、直径150μmの泡のような球状の孔が、直径40μmの連通孔で繋がっている。
製造方法は簡単であるが、ノーハウの塊である。アパタイトの細かい粉を水に溶かして掻き混ぜてスラリーとし、界面活性剤を加えて撹拌して泡状スラリーとする。それに重合剤を加えて泡構造を固定し、乾燥・加熱により多孔質焼結体とする方法である。
「ネオボーン」を骨に埋めると、連通孔から最初に血管が侵入する。次に骨を作る骨芽細胞が侵入してきて孔内に骨が再生される。体内で多孔体はいずれ壊れるが、骨ができているので問題は起きない。
「ネオボーン」の整形外科と歯科領域における応用に関し、大阪大学医学部付属病院未来医療センター副センター長の名井陽先生から情報を頂いた。2003年に厚労省から製造販売が承認され、最近は年間4,000症例くらいである(利益率は高いが決して大きい市場ではない)。14歳男性の上腕骨の良性骨腫瘍の症例では、「ネオボーン」の顆粒を移植して2か月経つと顆粒が繋がり、6か月経つと一体化し、腫れも引くようである。72歳女性の人工股関節再置換術の症例にも適用された。今の人工関節は回りの骨のゆるみで10~15年しかもたないので20~30年くらいもたせる研究がされている。現在は人工骨がゆるむと再置換術が行われている。手指中節骨内軟骨腫の症例では、「ネオボーン」の顆粒を移植して3か月で軽度の硬化、6か月で強い硬化が見られた。
多孔体は穴が沢山開いているので弱いという欠点がある。孔が開いているものと開いていないものを組み合わせたもの作ったのが、「NEOBONE-X」である。背骨の治療に使われる。
再生医療の研究は、大阪大学の吉川秀樹教授によって行われている。自家骨髄由来の細胞を培養しネオボーンに導入して骨疾患を治療する研究である。まず患者から血液と骨髄液を採取する。次に血液から栄養を取り出し、骨髄液から細胞を取り出して培養し、多孔体に入れて骨の治らない人に移植する方法で、現在、研究段階にある。
ネオボーンの研究開発を通して医工連携について学んだ。医学者は「骨再生を効果的に補助する人工骨」が必要であった。工学者は高い強度の多孔体を作りたい。良く似ているが、結局は違う。医療機器なので人体に入れるために安全でなければならない。そのため、医学者は新しい材料は使いたくない。古い材料で古い技術でも医学者は論文を書けるが、工学者は特許を書いても論文は書けない。医者と工学者のキャリアパスが違っているため、医工連携は難しい。医工連携には、お互いを尊敬し役割分担を理解することが大事であることを教わった。工学者は謙虚であるから医学者を尊敬することができるが、日本の医学者はアメリカと違って工学者を尊敬することはなかなか難しいらしい。最近は日本の医学者もそのことに気付き、お互いにリスペクトして役割分担しながら進めることができ始めているような気がする。この研究に参加した物質・材料研究機構の末次さんと菊地さんは主任研究員になりグループリーダーになっているのでキャリアパスとしては良かったと思うが、この材料に関して特許は出願したが論文は書いていない。
(2)血管侵入性の高い人工骨「リジェノス」
前節で紹介した「ネオボーン」は泡構造である。血管は壁に沿って侵入するが、連通孔のところでは進む方向が大きく変化し、次の孔への侵入が妨げられる。これがボトルネックとなって血管の侵入に時間が掛かる。そこで霜柱技術を使って一次元連通孔を形成した。アパタイトのスラリーを容器に入れ、底の金属板を冷却し、霜柱を成長させて氷の結晶の間にアパタイトを偏析させる。真空中で氷を昇華させれば、右図の構造のアパタイトができる。
この人工骨の開発は物質・材料研究機構と筑波大学整形外科の坂根先生との共同で行われた。2005年に基本設計を開始し、安全性試験を行ったのち承認申請し、2009年に製造販売の承認を取得した。臨床使用評価が行われ、2012年に㈱クラレから「リジェノス」として発売された。
この材料は血管の侵入は速い。しかし、強度は縦方向には強いが横方向には弱い。つまり、治りは早いが、手術中の取り扱いに注意が必要である。家兎の大腿骨髄腔に埋入したあとの連通孔方向の圧縮破断強度は、埋入前の13.4MPaから1年後に49.2MPaまで上昇し、2年経っても維持されることが分かった。最初強度が低くて使用するのがやや難しいが、治ってしまうと大丈夫である。
このような構造特性を活かしてリ「ジェノス」は、頸椎の椎弓形成用スペーサーに使われている。脊柱管内が狭くなって神経根を圧迫している症例では、椎弓の一部を切り取って広げて、そこにスペーサーとして「リジェノス」が使われている。
3.骨再生を促進する人工骨「リフィット」
(1)骨の構造と成分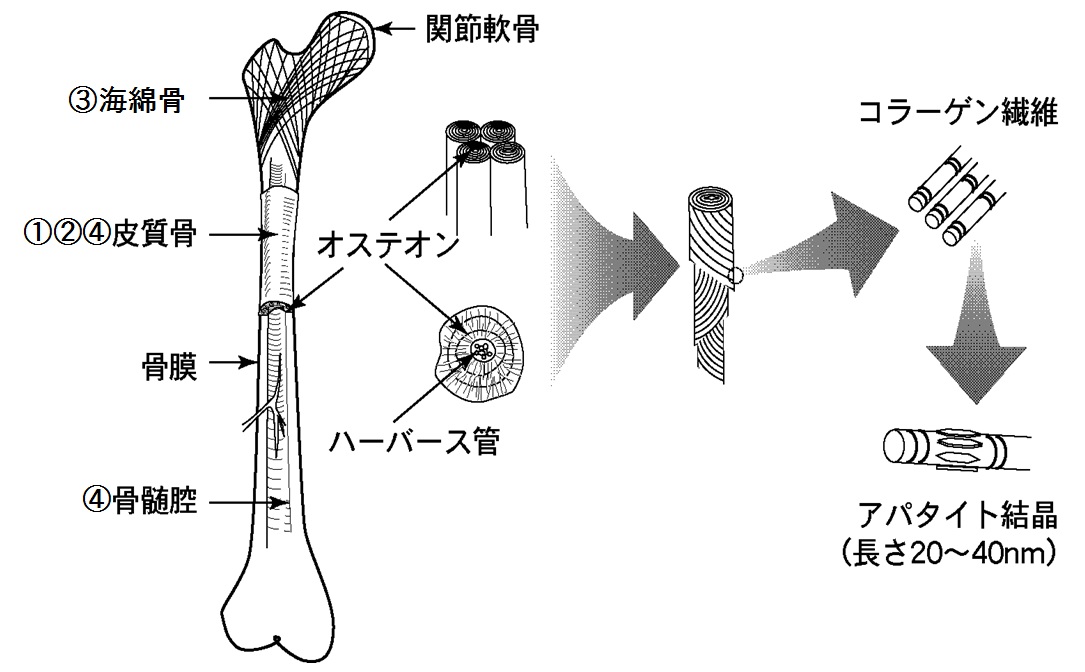
本当の骨に変わる人工骨を開発するためには、私達の骨の構造と成分から学ぶ必要がある。右図に大腿骨の階層構造を示す。細胞や栄養の素である骨膜の内側に最も硬い皮質骨がある。その内側に軟らかい海綿骨があり、真ん中に間葉系幹細胞の源になる骨髄腔が存在する。皮質骨を拡大してみると年輪状のオステオン(骨単位)からできている。年輪を剥いでみると、一つの層はコラーゲンの繊維が一方向に並んで巻いている。その下の層のコラーゲン繊維は上の層と直角方向に並んでいる。この構造はベニヤ板を巻いた構造になっており、皮質骨が高い強度を示す理由になっている。コラーゲン線維を拡大すると、300nmのコラーゲン線維の上に30 nmのアパタイト結晶が並んでいる。
現在は自己組織化という技術でコラーゲンとアパタイトを綺麗に並べることはでき、束にすることもできる。しかし、縦横に繊維の方向を交互に並べかえることができないため、オステオンの構造を作ることができない。マクロとナノテクの境界に大きな壁があり、そのため骨構造を再現できないでいる。
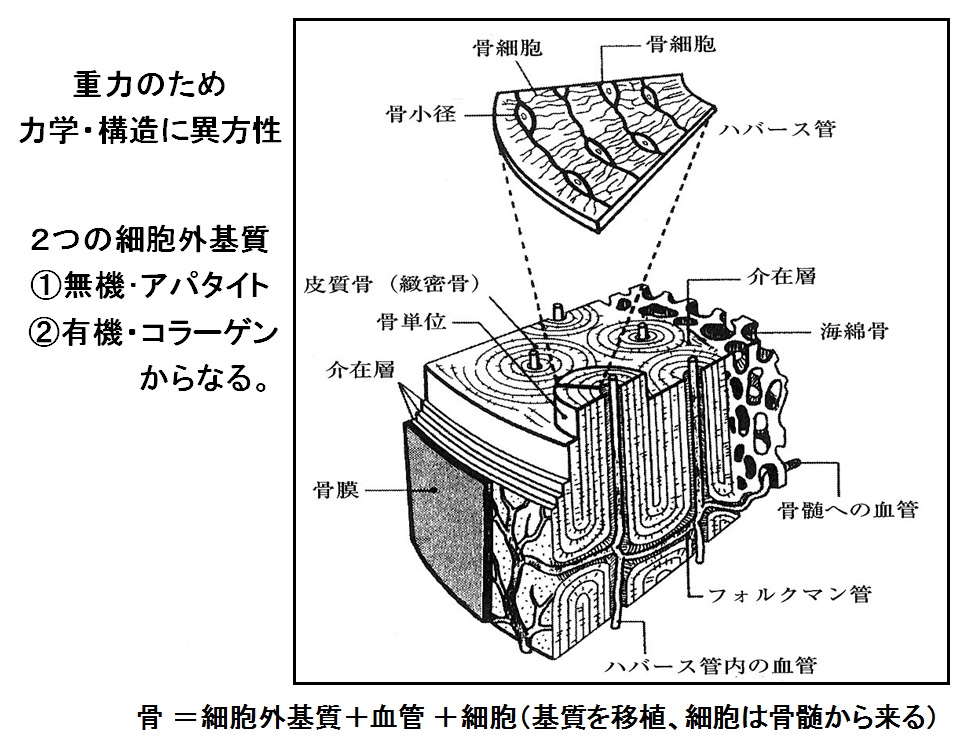
右図はより分かり易く書いた骨の微細構造である。オステオンの中央にはハバース管があり、その中を栄養や細胞が移動する。年輪の層間に骨細胞が存在する。骨細胞はセンサーの役目をしており、お互いに連携を取り合い、骨が壊れると骨芽細胞と破骨細胞を呼びよせて骨を作り替える。骨が作り替えられると、骨芽細胞は取り残されて骨細胞に変化する。
人の骨の無機成分であるアパタイトには5~6%の炭酸イオンが入っている。それに対して、焼結して作ったアパタイトには炭酸イオンは含まれていない。骨の炭酸イオンは、人間が呼吸してできた炭酸ガスが血液を介して骨に取り込まれたものである。アパタイトは非常に溶け難いが、炭酸イオンがあれば溶け易くなり、骨は作り替え易くなっている。また、骨のアパタイトの結晶性は低く、その点でも骨は作り替え易くなっている。最近は炭酸イオンを入れた材料や未焼成のアパタイトから骨を作る研究も行われている。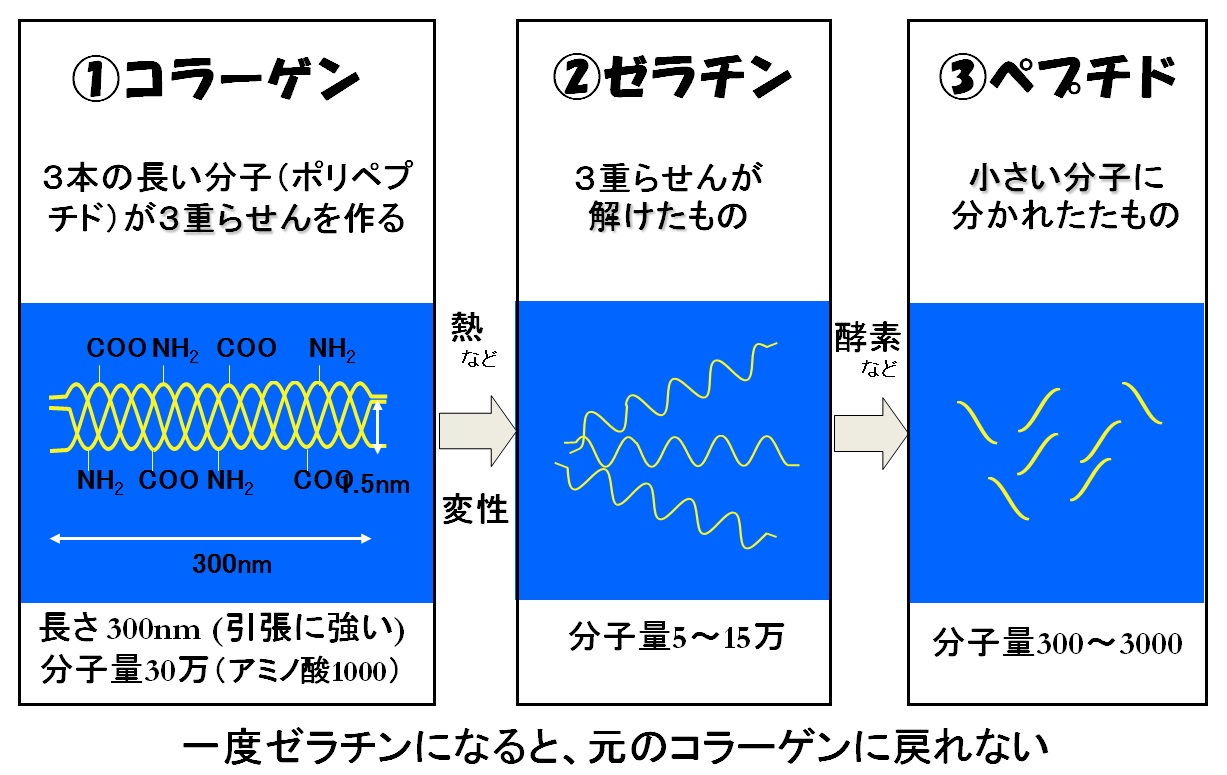
一方有機成分であるコラーゲンは、右図に示すように三本のたんぱく質(長いポリペプチド分子)が撚り合わされた三重らせん構造になっている。これがロープと同じように引張強度が高い理由である。現在、コラーゲンは牛骨か豚皮、または魚のウロコから作られている。コラーゲンの温度を上げると変性して三重らせんが解けたゼラチンになる。魚の煮こごりがゼラチンである。ゼラチンを酵素の働きでさらに小さい分子にしたものが、ペプチドである。アメリカのFDA(食品医薬品局)の下部機関で化粧品の名前を決めるINCIは、これらの三つを全てコラーゲンと命名して良いとしているので、コラーゲン入りの化粧品はこれらの三つの何れが含まれているのか分からない。
受精卵が分割した最初のある段階で胚性幹細胞(ES細胞)になる。この細胞は万能で、造血幹細胞や間葉系幹細胞などのあらゆる組織幹細胞になる。組織幹細胞は通常目立たないところにいて、怪我のときや異物が侵入したときに前面に出て活躍し始める。造血幹細胞は血液系の細胞に変わり、間葉系幹細胞は軟骨や骨を作る細胞に変わる。「リフィット」は間葉系幹細胞と非常に馴染みが良い。ES細胞を用いることは倫理的な問題があることから、山中教授が発見したiPS細胞を用いて間葉系幹細胞から骨を作る研究が大阪大学で行われている。
(2)開発の経過
骨再生を促進する人工骨の基礎研究は1987年に物質・材料研究機構で始まった。2000年から物質・材料研究機構と東京医科歯科大学の医工連携が始まり、2003年から企業(Pentax)が参加して開発が始まった。その後PentaxはHOYA に吸収されてHOYA
Technosurgicalとなり、薬事法の改正もあったが、2013年に薬事承認され、「リフィット」として製造販売が始まった。会社の吸収と薬事法の改正の二つの大きな波があったにも拘らず、長い時間を掛けて強い意志で実用化した人達を尊敬している。親会社のHOYAはアメリカナイズされた厳しい会社であるが、経営者は「リフィット」の販売に力を入れ、営業展開を図っている。昨年、開発に携わった関係者は社長表彰され、報われたと思っている。
基礎研究から始まった開発が30年間近く続けてこられたのは、東京医科歯科大学整形外科の四宮謙一教授(現在は横浜市立みなと赤十字病院の院長)が整形外科教室を完全に掌握し、基礎研究と応用研究のバランスをとって開発を行えたことによる。前に工学と医学が互いにリスペクトすることが大事であると述べたのは、四宮先生が念頭にあったからである。
(3)「リフィット」の特徴と作り方
「リフィット」はアパタイトとコラーゲンの複合体であるが、水に濡らすとスポンジ状の弾力性を示す。ナイフやハサミで容易に加工できるため、操作性に優れている。したがって、患部に詰め易く手術で使い易い。
試行錯誤を繰り返し、生体内で生じている自己組織化を利用すると、アパタイトとコラーゲンが綺麗に並んだ長さ3㎝くらいの骨の繊維ができることが分かった。前述した骨のリモデリング(第1項参照)において、骨芽細胞はコラーゲンを細胞内で作って細胞外に出す。その分子状のコラーゲンは並んで繊維を形成する。そこにリン酸とカルシウムが供給されて、コラーゲン繊維の上にアパタイトができ、アパタイトとコラーゲンが並んだ骨ができる仕組みである。
この生体内の仕組みを使うと骨に近い材料ができると考え、簡単なシステムを作って実験した。ビーカーに一方からリン酸とコラーゲンを注ぎ、もう一方から水酸化カルシウムを注いだ。この簡単な方法によって骨芽細胞の材料供給の仕組みを再現できる。温度は25、30、35、40℃と変化させ、pHはリン酸と水酸化カルシウムの注ぐ量を調整して7、8、9と変えた。その結果、温度40℃、pH8~9で最も骨に近い材料が得られた。pH8~9は体内pH7.3より少しアルカリ性の状態であるが、アパタイトが安定にできるpHである。また私たちの体温である40℃ではアパタイトとコラーゲンが自然に整列する(自己組織化する)温度であることが分かった。この温度40℃はコラーゲンがゼラチンに変わる変性温度で、コラーゲン分子の周りの水を放出してコラーゲン同士が強く相互作用する温度であった。
(4)リフィットの有効性の確認
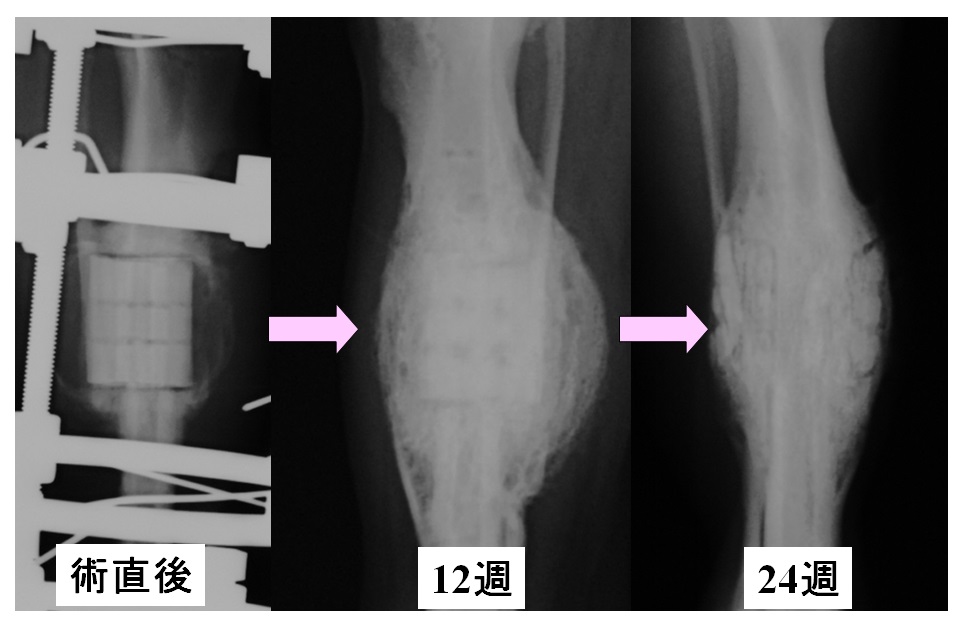 皮質骨の一部に欠陥を作って人工骨を移植した。その人工骨は時間の経過とともに吸収され周辺の骨と一体化して、12週間後には正常な骨に置き換わった。右図はビーグル犬の脛骨の一部に人工骨を入れギブスのようなもので固定した例である。レントゲン観察により、材料は吸収されて骨になり、上下の骨が繋がっていることが分かる。骨に似た性質を持った材料を入れると、生体は壊れた骨と判断して作り替え、本当の骨になることが確認された。 皮質骨の一部に欠陥を作って人工骨を移植した。その人工骨は時間の経過とともに吸収され周辺の骨と一体化して、12週間後には正常な骨に置き換わった。右図はビーグル犬の脛骨の一部に人工骨を入れギブスのようなもので固定した例である。レントゲン観察により、材料は吸収されて骨になり、上下の骨が繋がっていることが分かる。骨に似た性質を持った材料を入れると、生体は壊れた骨と判断して作り替え、本当の骨になることが確認された。
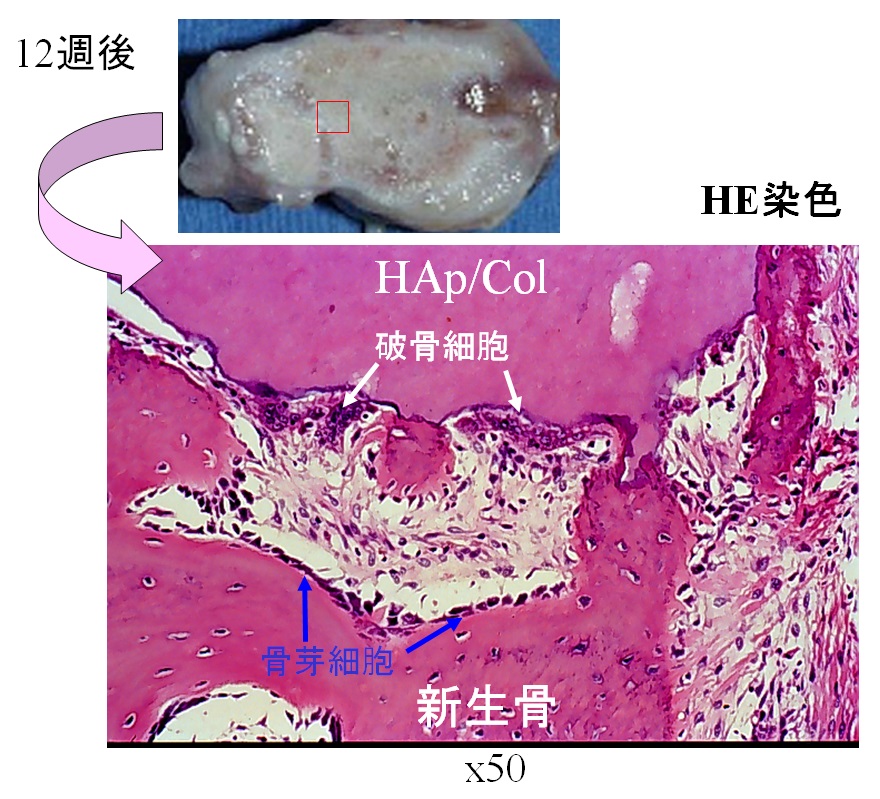 組織切片の内部を拡大した写真を右図に示す。染色してあるため白く見えるのが材料で、赤く見えるのが骨である。大きな細胞である破骨細胞が移植した人工骨を分解して(貪食して)できたカルシウムを使って骨芽細胞が骨を作っている。人工骨を壊れた骨と判断し、リモデリングが起こっている。3~6か月で人工骨は新しい本当の骨に変わる。 組織切片の内部を拡大した写真を右図に示す。染色してあるため白く見えるのが材料で、赤く見えるのが骨である。大きな細胞である破骨細胞が移植した人工骨を分解して(貪食して)できたカルシウムを使って骨芽細胞が骨を作っている。人工骨を壊れた骨と判断し、リモデリングが起こっている。3~6か月で人工骨は新しい本当の骨に変わる。
(5)臨床治験
東京医科歯科大学付属病院、慶応義塾大学付属病院、京都大学付属病院、帝京大学付属病院、癌研究会付属病院、国立がんセンター中央病院、土浦共同病院の七か所で臨床治験が行われた。33歳女性の左膝蓋骨良性腫瘍部にブロック8個(合計8mℓ)を補填した症例では、術後12週で周囲の骨との連続性および骨再生が確認された。59歳女性の尺骨の一部を採取して別のところに自家骨移植した例では、採取された尺骨の欠損部に「リフィット」のブロック2個(合計2mℓ)を補填した。その結果、術後24週で欠損部に骨が再生され、自家骨を採取した骨欠損の再生に適していることが示された。42歳男性の指の内軟骨腫の症例では、術後6か月で骨が再生され、腫れが引いている。
5.魚コラーゲンが面白い!
今までの話と変わるが、魚コラーゲンが面白い。牛や豚のウイルス(狂牛病など)は人間にうつるが、魚は人間と種が遠いので魚のウイルスは人間にうつっても直ぐに死んでしまう。そのため魚のコラーゲンは安全であり、ヨーロッパでは魚のコラーゲンしか化粧品に使えない。また、イスラム圏では豚、ヒンズー圏では牛の使用が禁忌である。魚は宗教的に問題がないので海外展開に有利である。日本では30社くらいが魚のコラーゲンを扱っている。
最初に骨を持った生物は約4億年前に現れた魚によく似た無顎類(甲冑魚など)である。無顎類のウロコ様組織はアスピディンと呼ばれ、それが進化して我々の骨や歯、魚のウロコになった。したがって私達の骨と魚のウロコは遠い親戚である。ウロコは何度抜けても生えてくる。サメの歯も次々入れ替わる。しかし人の歯は乳歯から永久歯にしか入れ替わらない。もともと骨も歯も再生する能力を持っていたが、歯は進化の過程で再生する方法を忘れてしまった。歯の再生は極めて難しく、現在も再生法は見つかっていない。
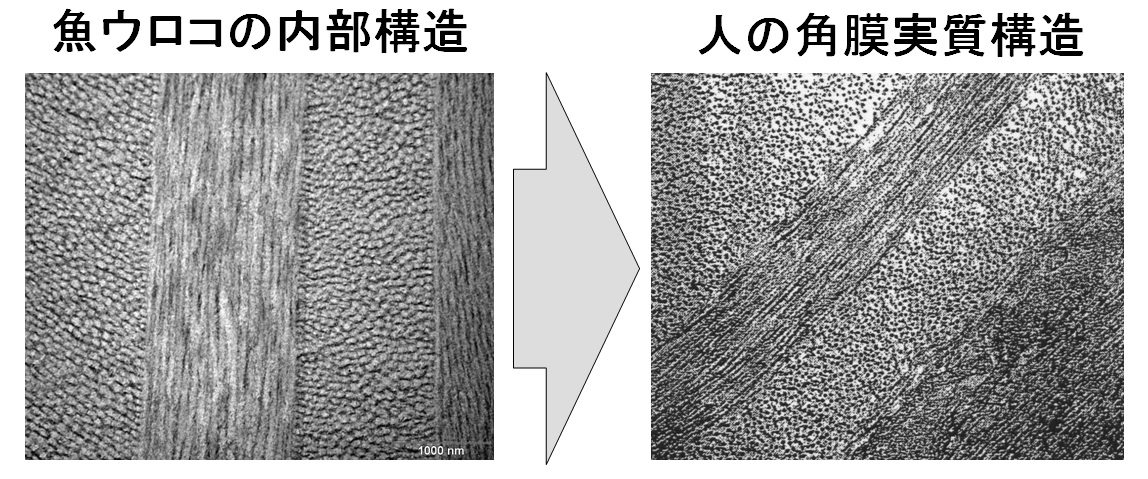 右図にウロコの内部構造を示す。コラーゲンが層状に縦横に並んだベニヤ板と同じような構造(層板構造)になっている。人間の眼の角膜実質も同じ構造を持っている。角膜実質は再生が難しいが、ウロコは抜けても類骨形成細胞によって約1週間で生えてくる。現在、類骨形成細胞を制御してコラーゲンを作る細胞の研究が行われている。ウロコのコラーゲンは作ることができるが、その分子の方向を揃えることができず、縦横の層板構造もできていない。前述したように骨のコラーゲンの構造も同じ層板構造で、人も魚も層板構造を作る方法が遺伝子の中に組み込まれている。将来、ウロコの類骨形成細胞の研究から、角膜実質や骨単位(オステオン)を再生できる可能性がある。なお、「目からウロコ」は日本の諺ではなく、聖書に載っている。 右図にウロコの内部構造を示す。コラーゲンが層状に縦横に並んだベニヤ板と同じような構造(層板構造)になっている。人間の眼の角膜実質も同じ構造を持っている。角膜実質は再生が難しいが、ウロコは抜けても類骨形成細胞によって約1週間で生えてくる。現在、類骨形成細胞を制御してコラーゲンを作る細胞の研究が行われている。ウロコのコラーゲンは作ることができるが、その分子の方向を揃えることができず、縦横の層板構造もできていない。前述したように骨のコラーゲンの構造も同じ層板構造で、人も魚も層板構造を作る方法が遺伝子の中に組み込まれている。将来、ウロコの類骨形成細胞の研究から、角膜実質や骨単位(オステオン)を再生できる可能性がある。なお、「目からウロコ」は日本の諺ではなく、聖書に載っている。
コラーゲンがゼラチンに変性する温度は、魚が生息する海や淡水の水温に比例している。低い水温に生息している魚(タラやサケなど)の変性温度は低く、高いところに生息する魚(テラピアなど)の変性温度は高い。このことが骨の作り易さと関係している。現在、生物の進化が遺伝子の視点から明らかにされつつある。
コラーゲンは化粧品として肌に付けると肌が綺麗になるというデータがあるが、今日は男性だけなので割愛する。
Q&A
Q1.股関節は再生することが可能か?
A1.関節には骨と軟骨があり、軟骨の再生は少しずつ進んできているが難しい。特に骨と軟骨を同時に再生することができない。現状では人工股関節が一番良いと思う。今日話した骨の再生は1㎝とかの小さな骨で、力の余り掛からないところしか治せない。
Q2.人体が血液型のように人工骨を受け入れる条件はあるか?
A2.自分の骨を移植するのは問題ないが、兄弟の骨でも異物反応を示す。薬物で処理すれば良いが、アメリカの会社が技術を持っており、教えて貰えない。液体窒素に浸して、コラーゲンの構造が変わると、構造由来の異物反応が起こり難くなる。骨のコラーゲンをバラバラにして異物反応が起きないようにし、人工的に作ったアパタイトと複合体にして人に移植すると治っていく。どうして治るかは極めて難しいが、コラーゲンのある部分に細胞が引っ付いて、その細胞に骨を作る指令が伝わり骨を作り始めるようである。
Q3.子供に人工骨を入れると成長とともに、人工骨が成長しなければならないが、そうなるか?
A3.子供に人工骨を使うと、本当の骨に変わらなければ奇形になる。「リフィット」は本当の骨に変わって成長するので、大人になって困ることはない。耳の小さい子がいるが、プラスティックの耳を作ってやれば、大人になってもそのままなので却っておかしいことになる。本当の軟骨に変わる骨の研究をしたことがあるが、コラーゲンと軟骨細胞を組み合わせて本当の軟骨にできる。現在、横浜市立大学などで研究が進んでいる。
Q4.骨の階層構造で縦横にコラーゲン線維が並んだ構造を作ることができないとのことであるが、どのような研究分野に属するか?
A4.縦横のコラーゲン線維の間に硫黄を含んだ小さい分子が存在し、それがコラーゲン線維を90°ずらしていると考えられる。そういう研究は材料分野で進められている。一方、東工大では細胞を用いて縦横の構造を作ろうとしている先生がいる。その研究分野は分子生物学である。
Q5.人工骨には血管の侵入が必要であるが、気泡のような侵入ルートが必要か?
A5.新生血管をいかに作るかは難しい。血管は壁に沿って伸びていくので、凹凸があると侵入し難く、霜柱構造が採用された。血管新生は幅広く研究されていて、非常に大事である。
(記録:池田)
|